เซลล์เชื้อเพลิง
จาก ChulaPedia
| (การแก้ไข 6 รุ่นระหว่างรุ่นที่เปรียบเทียบไม่แสดงผล) | |||
| แถว 1: | แถว 1: | ||
| - | + | == '''เซลล์เชื้อเพลิง (fuel cell)''' == | |
| + | |||
| + | เป็นกระบวนการเปลี่ยนรูปพลังงานจากพลังงานเคมีในสารตั้งต้นหรือเชื้อเพลิงไปเป็นพลังงานไฟฟ้าโดยอาศัยกระบวนการเคมีไฟฟ้า ซึ่งกระบวนการดังกล่าวมีประสิทธิภาพในการแปรรูปพลังงานสูงกว่ากระบวนการเผาไหม้ภายใน ส่งผลให้ช่วยลดการใช้เชื้อเพลิง นำไปสู่การลดการปลดปล่อยแก๊สคาร์บอนไดออกไซด์ซึ่งเป็นแก๊สเรือนกระจกออกสู่บรรยากาศ<ref>Larminie J. and Dicks A. (2003) Fuel Cell Systems Explained, 2nd ed., Wiley, Hoboken, NJ.</ref> เนื่องจากเชื้อเพลิงส่วนใหญ่ที่ใช้ในปัจจุบันมีธาตุคาร์บอนเป็นองค์ประกอบอยู่ ไม่ว่าจะเป็นถ่านหิน น้ำมัน หรือแม้แต่แก๊สธรรมชาติ สำหรับแนวคิดในอนาคตคือเซลล์เชื้อเพลิงจะขับเคลื่อนโดยใช้ไฮโดรเจนเป็นตัวพาพลังงาน ของเสียที่จะเกิดขึ้นจากการแปรรูปพลังงานจะมีเพียงความร้อนและน้ำเท่านั้น ดังนั้นถ้านำเซลล์เชื้อเพลิงมาใช้ในยานยนต์จะช่วยลดปริมาณแก๊สเรือนกระจกที่ปล่อยออกจากท่อไอเสียยานยนต์อย่างมาก | ||
| - | + | กระบวนการผลิตไฟฟ้าแบบดั้งเดิมจะดำเนินการโดยนำเชื้อเพลิงมาเผาให้ได้ความร้อน นำความร้อนไปขับเครื่องยนต์และพลังงานกลจากเครื่องยนต์ถูกนำไปใช้ในการปั่นไฟฟ้า ซึ่งทุกขั้นตอนของการแปรรูปพลังงานจากรูปแบบหนึ่งไปอีกรูปแบบหนึ่งมีการสูญเสีย การแปรรูปพลังงานผ่านกระบวนการเคมีไฟฟ้าในเซลล์เชื้อเพลิง ช่วยลดขั้นตอนเหล่านี้ลง จึงช่วงลดการสูญเสียและความซับซ้อนของกระบวนการ | |
| + | |||
| + | |||
| + | |||
| + | == '''ประเภทของเซลล์เชื้อเพลิง''' == | ||
| + | |||
| + | การจำแนกประเภทพิจารณาจากสารอิเล็กโทรไลต์ที่ใช้ โดยแบ่งได้เป็น 5ประเภทใหญ่ ได้แก่ | ||
| + | |||
| + | 1)เซลล์เชื้อเพลิงแบบกรดฟอสฟอริก (Phosphoric Acid Fuel Cell, PAFC) | ||
| + | |||
| + | 2)เซลล์เชื้อเพลิงแบบคาร์บอเนตหลอม (Molten Carbonate Fuel Cell, MCFC) | ||
| + | |||
| + | 3)เซลล์เชื้อเพลิงแบบออกไซด์แข็ง (Solid Oxide Fuel Cell, SOFC) | ||
| + | |||
| + | 4)เซลล์เชื้อเพลิงแบบอัลคาไลน์ (Alkaline Fuel Cell, AFC) | ||
| + | |||
| + | 5)เซลล์เชื้อเพลิงแบบเมมเบรนแลกเปลี่ยนโปรตอน (Proton Exchange Membrane Fuel Cell, PEMFC) และเซลล์เชื้อเพลิงแบบใช้เมทานอลโดยตรง (Direct Methanol Fuel Cell, DMFC) | ||
| + | |||
| + | เซลล์เชื้อเพลิงแต่ละประเภทจะมีช่วงการทำงานที่แตกต่างกัน เชื้อเพลิงที่ใช้อาจต่างกัน จึงเหมาะกับการใช้งานที่แตกต่างกันไป | ||
| + | |||
| + | |||
| + | [[ไฟล์:เซลล์เชื้อเพลิง01.JPG]] | ||
| + | |||
| + | |||
| + | |||
| + | == '''เซลล์เชื้อเพลิงชนิดเมมเบรนแลกเปลี่ยนโปรตอน''' == | ||
| + | |||
| + | เซลล์เชื้อเพลิงแบบเมมเบรนแลกเปลี่ยนโปรตอน เป็นเซลล์เชื้อเพลิงที่จะนำไปใช้ประโยชน์ในยานยนต์ เช่นเดียวกับเซลล์เคมีไฟฟ้าทั่วไป เซลล์เชื้อเพลิงประกอบด้วยขั้วไฟฟ้าสองขั้ว คือ ขั้วแอโนดและขั้วแคโทด โดยมีอิเล็กโทรไลต์ทำหน้าที่เป็นสะพานเชื่อมให้ไอออนที่เกิดขึ้นจากปฏิกิริยาเคมีไฟฟ้าสามารถเดินทางข้ามจากขั้วหนึ่งไปยังอีกขั้วไฟฟ้าหนึ่งได้ สำหรับเซลล์เชื้อเพลิงชนิดนี้ อิเล็กโทรไลต์เป็นพอลิเมอร์เมมเบรนที่ยอมให้โปรตอน (H+) ข้ามผ่านไป | ||
| + | |||
| + | ส่วนประกอบสำคัญที่ถือได้ว่าเป็นหัวใจของเซลล์เชื้อเพลิงแบบเมมเบรนแลกเปลี่ยนโปรตอน คือส่วนเมมเบรนประกอบขั้วไฟฟ้า หรือ Membrane Electrode Assembly (MEA) ซึ่งเป็นการนำขั้วไฟฟ้าแอโนดและแคโทดมาประกบกันโดยมีเมมเบรนนำไอออนแทรกอยู่ระหว่างกลาง ขั้วไฟฟ้าทั้งสองด้านเตรียมโดยจัดวางตัวเร่งปฏิกิริยาเคมีไฟฟ้าในปริมาณที่เหมาะสมลงบนขั้วไฟฟ้า ในกรณีนี้ตัวเร่งปฏิกิริยาคือแพลทินัม ซึ่งมักเตรียมอยู่บนผงคาร์บอน (Pt/C) โดย ตัวเร่งปฏิกิริยาเหล่านี้จะมีขนาด 2-10 นาโนเมตร ปฏิกิริยาที่เกิดขึ้น คือ ไฮโดรเจนที่ป้อนเข้ามา จะเกาะลงบนผิวของตัวเร่งปฏิกิริยา แล้วแตกตัวให้โปรตอนและอิเล็กตรอน อิเล็กตรอนเคลื่อนออกจากระบบผ่านสายไฟฟ้า ส่วนโปรตอนจะเคลื่อนที่ผ่านเมมเบรนโดยอาศัยการเคลื่อนที่ของน้ำภายในเมมเบรนข้ามมาฝั่งแคโทด ที่ซึ่งออกซิเจนที่ถูกป้อนเข้ามาจะมาเกาะลงบนตัวเร่งปฏิกิริยาและทำปฏิกิริยากับโปรตอนและอิเล็กตรอน ได้ผลผลิตเป็นน้ำและความร้อนดังแสดงในรูปที่ 1 รูปที่ 2 และ 3 เป็นรูปเซลล์เชื้อเพลิงสำหรับงานวิจัย ขนาด 5 ตร.ซม.และเซลล์เชื้อเพลิงการค้า ขนาด 1 กิโลวัตต์ ตามลำดับ | ||
| + | |||
| + | |||
| + | [[ไฟล์:เซลล์เชื้อเพลิง02.JPG]] | ||
| + | |||
| + | [[ไฟล์:เซลล์เชื้อเพลิง03.JPG]] | ||
| + | |||
| + | [[ไฟล์:เซลล์เชื้อเพลิง04.JPG]] | ||
| แถว 31: | แถว 69: | ||
[[ไฟล์:ลักษณะการทำงานของเซลล์เชื้อเพลิงชนิดออกไซด์แข็ง.jpg]] | [[ไฟล์:ลักษณะการทำงานของเซลล์เชื้อเพลิงชนิดออกไซด์แข็ง.jpg]] | ||
| - | ''ลักษณะการทำงานของเซลล์เชื้อเพลิงชนิดออกไซด์แข็ง | + | ''ลักษณะการทำงานของเซลล์เชื้อเพลิงชนิดออกไซด์แข็ง'' |
| + | |||
| + | |||
| + | == อ้างอิง == | ||
| + | <references/> | ||
'''อาจารย์ผู้ดูแลบทความ''' ผศ. ดร.อมรชัย อาภรณ์วิชานพ | '''อาจารย์ผู้ดูแลบทความ''' ผศ. ดร.อมรชัย อาภรณ์วิชานพ | ||
| - | อาจารย์ประจำภาควิชาวิศวกรรมเคมี | + | อาจารย์ประจำภาควิชาวิศวกรรมเคมี, หน่วยปฏิบัติการวิจัย การเปลี่ยนรูปพลังงานเคมี (Chemical Energy Conversion Research Unit) ภาควิชาเคมีเทคนิค คณะวิทยาศาสตร์ |
'''''ผู้รับผิดชอบบทความ''''' ศูนย์การสื่อสารนานาชาติแห่งจุฬาฯ | '''''ผู้รับผิดชอบบทความ''''' ศูนย์การสื่อสารนานาชาติแห่งจุฬาฯ | ||
รุ่นปัจจุบันของ 09:01, 25 มีนาคม 2554
เซลล์เชื้อเพลิง (fuel cell)
เป็นกระบวนการเปลี่ยนรูปพลังงานจากพลังงานเคมีในสารตั้งต้นหรือเชื้อเพลิงไปเป็นพลังงานไฟฟ้าโดยอาศัยกระบวนการเคมีไฟฟ้า ซึ่งกระบวนการดังกล่าวมีประสิทธิภาพในการแปรรูปพลังงานสูงกว่ากระบวนการเผาไหม้ภายใน ส่งผลให้ช่วยลดการใช้เชื้อเพลิง นำไปสู่การลดการปลดปล่อยแก๊สคาร์บอนไดออกไซด์ซึ่งเป็นแก๊สเรือนกระจกออกสู่บรรยากาศ[1] เนื่องจากเชื้อเพลิงส่วนใหญ่ที่ใช้ในปัจจุบันมีธาตุคาร์บอนเป็นองค์ประกอบอยู่ ไม่ว่าจะเป็นถ่านหิน น้ำมัน หรือแม้แต่แก๊สธรรมชาติ สำหรับแนวคิดในอนาคตคือเซลล์เชื้อเพลิงจะขับเคลื่อนโดยใช้ไฮโดรเจนเป็นตัวพาพลังงาน ของเสียที่จะเกิดขึ้นจากการแปรรูปพลังงานจะมีเพียงความร้อนและน้ำเท่านั้น ดังนั้นถ้านำเซลล์เชื้อเพลิงมาใช้ในยานยนต์จะช่วยลดปริมาณแก๊สเรือนกระจกที่ปล่อยออกจากท่อไอเสียยานยนต์อย่างมาก
กระบวนการผลิตไฟฟ้าแบบดั้งเดิมจะดำเนินการโดยนำเชื้อเพลิงมาเผาให้ได้ความร้อน นำความร้อนไปขับเครื่องยนต์และพลังงานกลจากเครื่องยนต์ถูกนำไปใช้ในการปั่นไฟฟ้า ซึ่งทุกขั้นตอนของการแปรรูปพลังงานจากรูปแบบหนึ่งไปอีกรูปแบบหนึ่งมีการสูญเสีย การแปรรูปพลังงานผ่านกระบวนการเคมีไฟฟ้าในเซลล์เชื้อเพลิง ช่วยลดขั้นตอนเหล่านี้ลง จึงช่วงลดการสูญเสียและความซับซ้อนของกระบวนการ
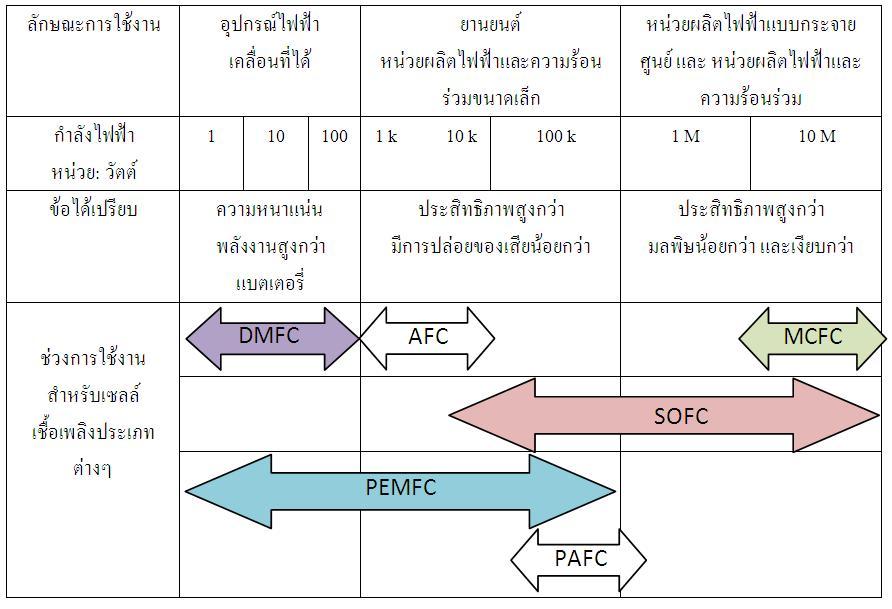
ประเภทของเซลล์เชื้อเพลิง
การจำแนกประเภทพิจารณาจากสารอิเล็กโทรไลต์ที่ใช้ โดยแบ่งได้เป็น 5ประเภทใหญ่ ได้แก่
1)เซลล์เชื้อเพลิงแบบกรดฟอสฟอริก (Phosphoric Acid Fuel Cell, PAFC)
2)เซลล์เชื้อเพลิงแบบคาร์บอเนตหลอม (Molten Carbonate Fuel Cell, MCFC)
3)เซลล์เชื้อเพลิงแบบออกไซด์แข็ง (Solid Oxide Fuel Cell, SOFC)
4)เซลล์เชื้อเพลิงแบบอัลคาไลน์ (Alkaline Fuel Cell, AFC)
5)เซลล์เชื้อเพลิงแบบเมมเบรนแลกเปลี่ยนโปรตอน (Proton Exchange Membrane Fuel Cell, PEMFC) และเซลล์เชื้อเพลิงแบบใช้เมทานอลโดยตรง (Direct Methanol Fuel Cell, DMFC)
เซลล์เชื้อเพลิงแต่ละประเภทจะมีช่วงการทำงานที่แตกต่างกัน เชื้อเพลิงที่ใช้อาจต่างกัน จึงเหมาะกับการใช้งานที่แตกต่างกันไป
เซลล์เชื้อเพลิงชนิดเมมเบรนแลกเปลี่ยนโปรตอน
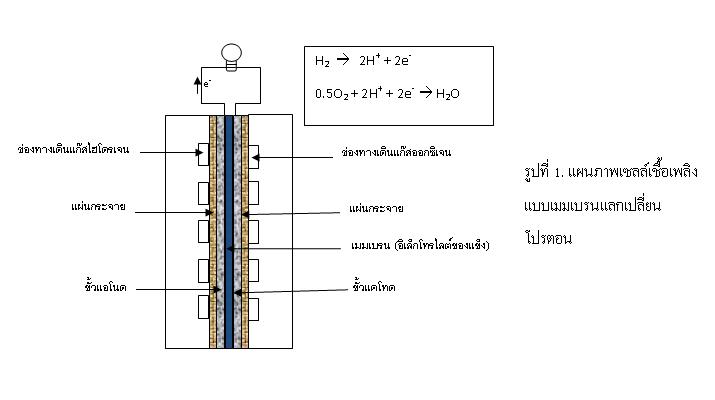
เซลล์เชื้อเพลิงแบบเมมเบรนแลกเปลี่ยนโปรตอน เป็นเซลล์เชื้อเพลิงที่จะนำไปใช้ประโยชน์ในยานยนต์ เช่นเดียวกับเซลล์เคมีไฟฟ้าทั่วไป เซลล์เชื้อเพลิงประกอบด้วยขั้วไฟฟ้าสองขั้ว คือ ขั้วแอโนดและขั้วแคโทด โดยมีอิเล็กโทรไลต์ทำหน้าที่เป็นสะพานเชื่อมให้ไอออนที่เกิดขึ้นจากปฏิกิริยาเคมีไฟฟ้าสามารถเดินทางข้ามจากขั้วหนึ่งไปยังอีกขั้วไฟฟ้าหนึ่งได้ สำหรับเซลล์เชื้อเพลิงชนิดนี้ อิเล็กโทรไลต์เป็นพอลิเมอร์เมมเบรนที่ยอมให้โปรตอน (H+) ข้ามผ่านไป
ส่วนประกอบสำคัญที่ถือได้ว่าเป็นหัวใจของเซลล์เชื้อเพลิงแบบเมมเบรนแลกเปลี่ยนโปรตอน คือส่วนเมมเบรนประกอบขั้วไฟฟ้า หรือ Membrane Electrode Assembly (MEA) ซึ่งเป็นการนำขั้วไฟฟ้าแอโนดและแคโทดมาประกบกันโดยมีเมมเบรนนำไอออนแทรกอยู่ระหว่างกลาง ขั้วไฟฟ้าทั้งสองด้านเตรียมโดยจัดวางตัวเร่งปฏิกิริยาเคมีไฟฟ้าในปริมาณที่เหมาะสมลงบนขั้วไฟฟ้า ในกรณีนี้ตัวเร่งปฏิกิริยาคือแพลทินัม ซึ่งมักเตรียมอยู่บนผงคาร์บอน (Pt/C) โดย ตัวเร่งปฏิกิริยาเหล่านี้จะมีขนาด 2-10 นาโนเมตร ปฏิกิริยาที่เกิดขึ้น คือ ไฮโดรเจนที่ป้อนเข้ามา จะเกาะลงบนผิวของตัวเร่งปฏิกิริยา แล้วแตกตัวให้โปรตอนและอิเล็กตรอน อิเล็กตรอนเคลื่อนออกจากระบบผ่านสายไฟฟ้า ส่วนโปรตอนจะเคลื่อนที่ผ่านเมมเบรนโดยอาศัยการเคลื่อนที่ของน้ำภายในเมมเบรนข้ามมาฝั่งแคโทด ที่ซึ่งออกซิเจนที่ถูกป้อนเข้ามาจะมาเกาะลงบนตัวเร่งปฏิกิริยาและทำปฏิกิริยากับโปรตอนและอิเล็กตรอน ได้ผลผลิตเป็นน้ำและความร้อนดังแสดงในรูปที่ 1 รูปที่ 2 และ 3 เป็นรูปเซลล์เชื้อเพลิงสำหรับงานวิจัย ขนาด 5 ตร.ซม.และเซลล์เชื้อเพลิงการค้า ขนาด 1 กิโลวัตต์ ตามลำดับ
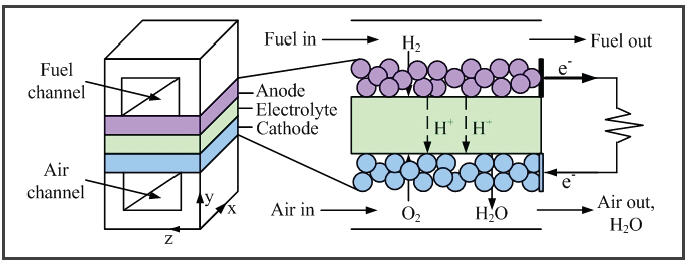
เซลล์เชื้อเพลิงชนิดออกไซด์แข็ง (Solid Oxide Fuel Cell, SOFC)
เซลล์เชื้อเพลิงชนิดออกไซด์แข็งเป็นเซลล์เชื้อเพลิงประเภทหนึ่งที่ใช้ในการผลิตพลังงานไฟฟ้าที่มีประสิทธิภาพสูง เนื่องจากเซลล์เชื้อเพลิงชนิดออกไซด์แข็งทำงานที่อุณหภูมิสูง ทำให้การออกแบบ การดำเนินงาน และการควบคุมเซลล์เชื้อเพลิงมักมีความซับซ้อน ทั้งนี้ปัญหาที่พบ ได้แก่ เซลล์เชื้อเพลิงอาจเกิดการแตกหักเนื่องจากเกิดความเค้นภายในหรือเกิดการขยายตัวทางความร้อนของวัสดุที่ใช้ภายในเซลล์ นอกจากนี้ยังจำเป็นต้องเลือกใช้วัสดุที่สามารถทนอุณหภูมิสูงได้ ทำให้ค่าใช้จ่ายในการสร้างเซลล์เชื้อเพลิงสูง รวมทั้งอาจมีผลต่ออายุการใช้งานของเซลล์เชื้อเพลิงด้วย
ภาพลักษณะการทำงานของเซลล์เชื้อเพลิงชนิดออกไซด์แข็ง
ข้อจำกัดและแนวทางการพัฒนาเซลล์เชื้อเพลิงชนิดออกไซด์แข็ง
เนื่องจากเซลล์เชื้อเพลิงชนิดออกไซด์แข็งทำงานที่อุณหภูมิสูง ทำให้การออกแบบ การดำเนินงาน และการควบคุมเซลล์เชื้อเพลิงมักมีความซับซ้อน ทั้งนี้ปัญหาที่พบ ได้แก่ เซลล์เชื้อเพลิงอาจเกิดการแตกหักเนื่องจากเกิดความเค้นภายในหรือเกิดการขยายตัวทางความร้อนของวัสดุที่ใช้ภายในเซลล์ นอกจากนี้ยังจำเป็นต้องเลือกใช้วัสดุที่สามารถทนอุณหภูมิสูงได้ ทำให้ค่าใช้จ่ายในการสร้างเซลล์เชื้อเพลิงสูง รวมทั้งอาจมีผลต่ออายุการใช้งานของเซลล์เชื้อเพลิงด้วย
การใช้เซลล์เชื้อเพลิงแบบที่ใช้ขั้วอิเล็กโทรดเป็นโครงสร้างรองรับ
ขั้วแอโนดจะเป็นองค์ประกอบที่หนาที่สุดและทำหน้าที่เป็นโครงสร้างรองรับ ในขณะที่ชั้นอิเล็กโทรไลต์มีขนาดบางที่สุด ทำให้ค่าศักย์ไฟฟ้าสูญเสียเนื่องจากความต้านทานไฟฟ้า (ohmic loss) ลดลง อย่างไรก็ตามเมื่อพิจารณาสมรรถนะทางไฟฟ้าของเซลล์เชื้อเพลิงที่ใช้ขั้วแอโนดเป็นโครงสร้างรองรับ พบว่าค่าศักย์ไฟฟ้าสูญเสียเนื่องจากปฏิกิริยาไฟฟ้าเคมี (activation loss) และค่าศักย์ไฟฟ้าสูญเสียเนื่องจากผลของการถ่ายโอนมวล (concentration loss) อาจมีค่ามากกว่าค่าศักย์ไฟฟ้าสูญเสียเนื่องจากความต้านทานไฟฟ้าที่ลดลงเนื่องจากการใช้ชั้นอิเล็กโทรไลต์ที่บางลง ทำให้เซลล์เชื้อเพลิงที่ใช้ขั้วแอโนดเป็นโครงสร้างรองรับและดำเนินงานด้วยอุณหภูมิปานกลางอาจมีค่าความต้านทานจำเพาะมากกว่าเซลล์เชื้อเพลิงที่ดำเนินงานที่อุณหภูมิสูง ดังนั้นจึงมีความพยายามที่จะพัฒนาอิเล็กโทรดและอิเล็กโทรไลต์ โดยมุ่งเน้นที่จะให้เซลล์เชื้อเพลิงมีสมรรถนะที่ดีขึ้น ภายใต้การดำเนินงานด้วยอุณหภูมิที่ต่ำลง
การพัฒนาอิเล็กโทรไลต์ชนิดใหม่สำหรับเซลล์เชื้อเพลิงชนิดออกไซด์แข็ง
เป็นอีกแนวทางหนึ่งในการลดค่าศักย์ไฟฟ้าสูญเสียเนื่องจากความต้านทานไฟฟ้าที่สูงขึ้นภายใต้การดำเนินงานที่อุณหภูมิปานกลาง โดยทั่วไปเซลล์เชื้อเพลิงชนิดนี้สามารถใช้อิเล็กโทรไลต์ได้ 2 ประเภท คือ อิเล็กโทรไลต์ที่มีความสามารถในการนำออกซิเจนไอออน (oxygen ion conducting) และอิเล็กโทรไลต์ที่มีความสามารถในการนำโปรตอน (proton conducting) ความแตกต่างหลักระหว่างการใช้อิเล็กโทรไลต์ทั้ง 2 ชนิดคือตำแหน่งของการเกิดน้ำที่ได้จากเซลล์เชื้อเพลิง สำหรับเซลล์เชื้อเพลิงที่มีความสามารถในการนำออกซิเจนไอออน น้ำจะเกิดขึ้นทางด้านขั้วแอโนด ในขณะที่เซลล์เชื้อเพลิงที่มีความสามารถในการนำโปรตอน น้ำจะ เกิดขึ้นทางด้านขั้วแคโทด ที่ผ่านมาพบว่างานวิจัยส่วนใหญ่มุ่งเน้นศึกษาเซลล์เชื้อเพลิงชนิดออกไซด์แข็งที่ใช้อิเล็กโทรไลต์ที่มีความสามารถในการนำออกซิเจนไอออนเพราะมีความเสถียรภาพทางเคมีและมีความต้านทานต่ำ อย่างไรก็ตาม เนื่องจากน้ำที่เกิดขึ้นทางด้านแอโนดจะทำให้ความเข้มข้นของไฮโดรเจนเจือจางลง ส่งผลทำให้ค่าศักย์ไฟฟ้าที่ได้ลดลง นอกจากนี้ยังต้องเสียค่าใช้จ่ายในการนำเชื้อเพลิงที่เหลือกลับมาใช้ประโยชน์ เนื่องจากในปัจจุบันมีการพัฒนาออกไซด์แข็งที่มีความสามารถในการนำโปรตอน ส่งผลให้นักวิจัยบางส่วนเริ่มหันมาสนใจศึกษาเซลล์เชื้อเพลิงชนิดออกไซด์แข็งแบบที่ใช้อิเล็กโทรไลต์ที่มีความสามารถในการนำโปรตอน โดยทั่วไปอิเล็กโทรไลต์ที่มีความสามารถในการนำโปรตอนมักใช้กับเซลล์เชื้อเพลิงที่ดำเนินงานที่อุณหภูมิต่ำ เช่น เซลล์เชื้อเพลิงชนิดเยื่อแผ่นแลกเปลี่ยนโปรตอน ดังนั้นการประยุกต์ใช้อิเล็กโทรไลต์ที่มีความสามารถในการนำโปรตอนกับเซลล์เชื้อเพลิงชนิดออกไซด์แข็งจึงมีความน่าสนใจ
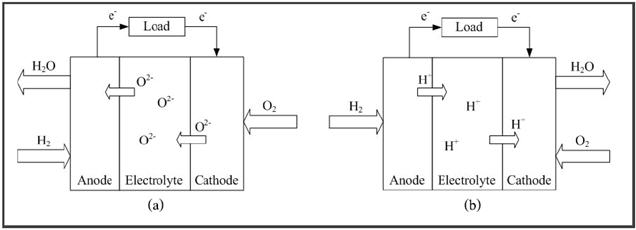 ลักษณะการทำงานของเซลล์เชื้อเพลิงชนิดออกไซด์แข็ง
ลักษณะการทำงานของเซลล์เชื้อเพลิงชนิดออกไซด์แข็ง
อ้างอิง
- ↑ Larminie J. and Dicks A. (2003) Fuel Cell Systems Explained, 2nd ed., Wiley, Hoboken, NJ.
อาจารย์ผู้ดูแลบทความ ผศ. ดร.อมรชัย อาภรณ์วิชานพ
อาจารย์ประจำภาควิชาวิศวกรรมเคมี, หน่วยปฏิบัติการวิจัย การเปลี่ยนรูปพลังงานเคมี (Chemical Energy Conversion Research Unit) ภาควิชาเคมีเทคนิค คณะวิทยาศาสตร์
ผู้รับผิดชอบบทความ ศูนย์การสื่อสารนานาชาติแห่งจุฬาฯ